Angeborene und erworbene Störungen der Thrombozyten
Angeborene und erworbene Thrombozytopenien (kritisch verminderte Anzahl an Blutplättchen im Blut) oder Thrombozytopathien (veränderte Blutplättchenfunktion) bilden häufig die Ursache für unkontrollierte Blutungen. Diese sind meist von milder Ausprägung und somit schwer detektierbar. Somit besteht eine entscheidende Relevanz Thrombozytendefekte bereits im Kindesalter präzise zu diagnostizieren, um Alltagsrisiken für unvorhergesehen schwere Blutungen zu minimieren oder die perioperative Versorgung von Patienten zu gewährleisten.
Wir untersuchen im Kontext mit der Diagnose von unklaren (syndromalen) Blutungserkrankungen mit Ursache in Thrombozytopenien und/oder –pathien die (fehlgesteuerte) Genese von Thrombozyten aus Megakaryozyten. Als Modelsystem dient uns dabei das Thrombocytopenia absent radii (TAR)- Syndrom, für welches die genetische Ursache von uns hinreichend aufgeschlüsselt wurde (Klopocki, Schulze H, et al., AJHG, 2007; Albers, …, Schulze H, et al., Nature Genetics, 2012). Dabei fokussieren wir uns auf Gendosisdefekte während der Reifung von humanen hämatopoietischen Stammzellen zu Thrombozyten-abschnürenden Megakaryozyten in Kultur. Dafür nutzen wir CD34-positive Zellen aus Gesundspender-Leukapheresen und manipulieren diese mittels lentiviraler Transduktion von shRNA-tragenden Vektorsystemen. Zusätzliche bedienen wir uns induzierter pluripotenter Stammzellen (iPS) aus Patienten, für die wir ein Megakaryozyten-Differenzierungsprotokoll etabliert haben. Somit lassen sich Defekte während der Reifung von humanen Megakaryozyten bis hin zu Thrombozyten-ähnlichen Fragmenten in vitro nachverfolgen.
Thrombozyten und Sepsis
Sepsis ist eine schwere Erkrankung, welche aus einem komplizierten Zusammenspiel des Körpers und Bakterien oder Pilzen entsteht. Sie ist mit weltweit 20-30 Millionen Neuerkrankungen ein sehr häufiges Krankheitsbild. Im Krankheitsverlauf erliegen viele Patienten der Erkrankung.
In enger Zusammenarbeit mit der Intensivstation des Universitätsklinikums Würzburg untersuchen wir die Veränderungen, die im Blutplättchen von Patienten mit Sepsis auftreten. Sepsis ist ein sehr schlecht verstandenes Krankheitsbild, zu dessen Aufklärung wir unseren Beitrag leisten wollen.
Blutplättchen (Thrombozyten) entstehen aus Megakaryozyten (grün), die an Gefäßen (rot) im Knochen (blau) liegen
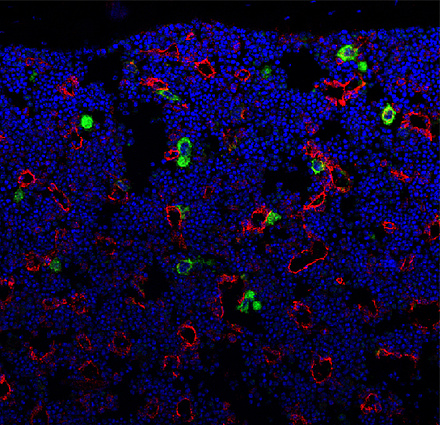
Blutplättchen gehören zu den zellulären Bestandteilen des Blutes und sind im wesentlichen für die Stillung von Blutungen verantwortlich. Der Mensch besitzt normalerweise zwischen 150000 und 400000 Blutplättchen in jedem ul Blut. Bei einem Mangel von unter 150000 spricht man von einer Thrombozytopenie und man findet oft eine verstärkte Blutungsneigung. Dieser Mangel kann erworben sein, zum Beispiel durch Medikamente wie Heparin oder die Bildung von Antikörpern gegen Plättchen nach Infektionen. Bei den angeborenen Thrombozytopenien liegen Defekte auf genetischer Ebene vor, die zu einem Mangel an Blutplättchen führen.
Jeweils ca. 1000 Blutplättchen werden als kernlose Abschnürungen aus den Vorläuferzellen im Knochenmark, den sogenannten Megakaryozyten, in den Blutstrom abgegeben. Bei diesem zellbiologischen Vorgang bekommt jedes Plättchen das zytoskeletäre Gerüst aus Mikrotubuli, das ihm seine diskoide Form verleiht. Zudem besitzt jedes Plättchen verschiedene Granula, die bei Gefäßverletzung freigesetzt werden und somit helfen, den Blutverlust zu stoppen.
Unsere Arbeitsgruppe beschäftigt sich zum einen mit den biologischen Grundlagen, die die Abschnürung von Blutplättchen aus Megakaryozyten erklären. Ein weiterer Fokus des Labors sind die seltenen angeborenen Bildungsstörungen von Blutplättchen wie z.B. das TAR-Syndrom.
Im Rahmen von Transplantationen solider Organe untersuchen wir den Einfluss von Antikörpern gegen HLA-Merkmale auf eine mögliche Organabstoßung. Bei hämatopoetischen Stammzelltransplantationen sind wir an Mechanismen interessiert, die zum Transplantversagen führen oder zu einer schweren GvH-Erkrankung.
Forschungsförderung
Das Labor wird unterstützt durch:
Deutsche Forschungsgemeinschaft DFG
DFG: TransRegio 240 "Thrombozyten"
Günter-Landbeck Excellence Award
weitere Mittelgeber waren:
Juniorforschergruppe Pädiatrie der Emil Alexander Hübner und Gemahlin-Stiftung Stifterverband

